Paano makapasa sa isang pagsusulit sa kimika

Nilalaman
- yugto
- Bahagi 1 Pagbubuo ng Magandang Gawi sa Pag-aaral
- Bahagi 2 Pag-unawa sa Mga istruktura ng Atomic
- Bahagi 3 Pagsula ng Chemical Reaction
- Bahagi 4 Paglalapat ng Matematika sa Chemistry
- Bahagi 5 Gamit ang wika ng kimika
Upang magtagumpay sa isang pangkalahatang kurso ng kimika, dapat mong maunawaan ang mga pundasyon ng paksang ito, magagawang gumawa ng mga simpleng kalkulasyon, gumamit ng isang calculator upang maisagawa ang mas kumplikadong mga operasyon at maging handa na matuto ng ibang kakaiba. Ang kimika ay isang agham na nag-aaral ng bagay at mga katangian nito. Ang lahat sa paligid sa amin ay nauugnay sa kimika, kahit na ang pinaka pangunahing mga bagay na maaari mong isaalang-alang na medyo natural, tulad ng tubig na inumin mo at ang mga katangian ng hangin na iyong hininga. Manatiling bukas sa bagong kaalaman pagdating sa pag-unawa sa mundo sa paligid mo, kahit na sa antas ng atomic. Ang iyong unang pakikipag-ugnay sa kimika ay maaaring maging mapaghamong at kapana-panabik.
yugto
Bahagi 1 Pagbubuo ng Magandang Gawi sa Pag-aaral
-

Alamin na makilala ang iyong guro. Upang magtagumpay sa klase ng kimika at makakuha ng mas mahusay na mga marka sa klase, gumugol ng oras upang matugunan ang iyong guro at ibahagi sa kanya ang hindi mo maintindihan.- Maraming mga guro ang may mga gabay sa pag-aaral at handang tumanggap ng mga mag-aaral sa labas ng oras ng paaralan kung kinakailangan.
-

Bumuo o sumali sa isang pangkat ng pag-aaral. Huwag mahihiya kung nakita mo na kumplikado ang mga kurso sa kimika. Ito ay isang mahirap na paksa para sa halos lahat.- Kung sumali ka sa isang grupo, ang ilang mga miyembro ay maaaring makahanap ng mga bahagi ng kurso na mas madali kaysa sa iba at maaaring ibahagi ang kanilang mga pamamaraan sa pagkatuto sa lahat. Hatiin ang mga gawain.
-

Basahin ang mga kabanata. Ang mga aklat-aralin sa kimika ay hindi palaging ang pinaka-kapana-panabik na mga libro na basahin. Gayunpaman, dapat mong maglaan ng oras upang basahin ang mga klasiko na ibinigay sa iyo, at i-highlight ang mga bahagi na hindi mo maintindihan. Subukang gumawa ng isang listahan ng mga katanungan o konsepto na hindi mo maintindihan.- Subukang maglaon upang basahin muli ang mga mahirap unawain na mga bahagi. Kung hindi mo pa rin sila naiintindihan, talakayin sila sa iyong pangkat ng pag-aaral, iyong guro o iyong katulong na propesor.
-

Sagutin ang mga tanong sa survey. Kahit na mayroon kang impresyon na mapuspos ng lahat ng mga dokumento na pinag-aralan mo, alamin na maaari mong naalala ang higit pang mga konsepto kaysa sa iniisip mo. Sagutin ang mga tanong sa pagtatapos ng mga kabanata.- Karamihan sa mga aklat-aralin ay nagbibigay ng iba pang impormasyon tungkol sa kung paano makahanap ng tamang sagot. Papayagan ka nitong makita kung ano ang iyong napalampas sa iyong pangangatuwiran.
-

Suriin ang mga diagram, larawan, at mga talahanayan. Madalas kang makakakita ng mga visual sa mga aklat-aralin na makakatulong sa iyo na mas maunawaan ang mga pangunahing elemento na dapat tandaan.- Tingnan ang mga larawan at mga caption na kasama nito. Makakatulong ito sa iyo na maunawaan ang ilang mga konsepto.
-

Humingi ng pahintulot upang irehistro ang kurso. Mahirap na kumuha ng mga tala sa isang kuwaderno at sa parehong oras tingnan kung ano ang nakasulat sa board, lalo na ang isang kumplikadong kurso tulad ng kimika. -

Subukang magkaroon ng mga lumang patunay at lumang manual. Pinapayagan ng karamihan sa mga paaralan ang mga mag-aaral na magkaroon ng lehitimo para sa mga lumang pagsusulit upang matulungan silang maghanda para sa mga pagsusulit.- Iwasan ang pagsasaulo ng mga sagot. Sa kimika, kung nais mong masagot ang parehong tanong sa iba't ibang mga termino, dapat mong maunawaan ang mga konsepto.
-

Suriin ang mga mapagkukunan ng tulong sa online. Suriin ang anumang mga link o mga mapagkukunang online na ibinigay ng kagawaran ng kimika ng iyong institusyon.
Bahagi 2 Pag-unawa sa Mga istruktura ng Atomic
-

Magsimula sa pinaka pangunahing mga istruktura. Upang makapasa ng isang pagsusulit sa kimika, dapat mong maunawaan ang mga pangunahing elemento na bumubuo sa lahat ng bagay na mayroong sangkap o masa.- Ang pag-unawa sa istraktura ng pinakamahalagang elemento sa kimika, iyon ay, latome, ay ang unang hakbang sa pag-unawa sa disiplina na ito. Ang lahat ng mga paksang tatalakayin sa klase ay magiging isang extension ng pangunahing impormasyon na ito. Kumuha ng oras na kinakailangan upang maunawaan ang atomic chemistry.
-
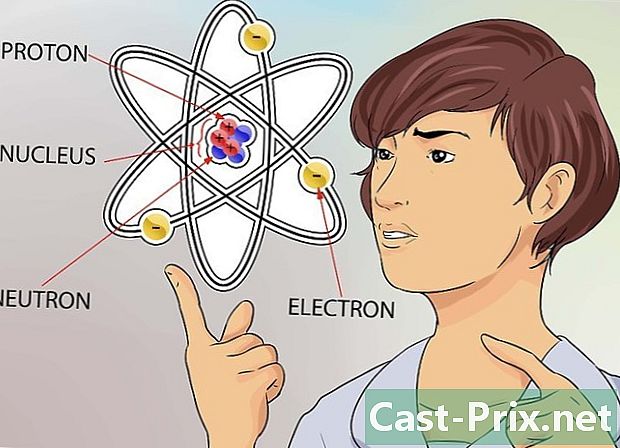
Maunawaan ang konsepto ng datome. Ang Latome ay itinuturing na pinakamaliit na constitutive element ng lahat ng bagay, kabilang ang mga bagay na hindi natin laging nakikita, tulad ng mga gas. Gayunpaman, kahit na ang isang maliit na atom ay binubuo ng kahit na mas maliit na mga particle na bumubuo sa istraktura nito.- Ang atom ay binubuo ng mga neutron, proton at elektron. Ang sentro ng latome ay tinatawag na nucleus, at ang isang ito ay binubuo ng mga neutron at proton. Ang mga electron ay ang mga partikulo na nag-iiba-iba sa latome, tulad ng mga planeta na umiikot sa paligid ng araw.
- Ang laki ng isang atom ay hindi kapani-paniwalang maliit, ngunit upang mabigyan ka ng isang paghahambing, subukang isipin ang pinakamalaking istadyum na alam mo. Kung isasaalang-alang mo ang yugtong ito bilang isang atom, ang nucleus ay magiging kasing laki ng isang pea na inilagay sa gitna ng bukid.
-
Maunawaan ang istraktura ng atomic ng isang elemento. Ang term elemento ay tinukoy bilang isang natural na nagaganap na sangkap na hindi masisira sa iba pang mga pangunahing elemento at nasa pinakasimpleng anyo nito. Ang mga elemento ay binubuo ng mga datom.- Ang mga atomo na naroroon sa isang elemento ay magkapareho. Nangangahulugan ito na ang bawat elemento, sa istraktura ng atomic nito, ay may kilala at natatanging bilang ng mga neutron at proton.
-
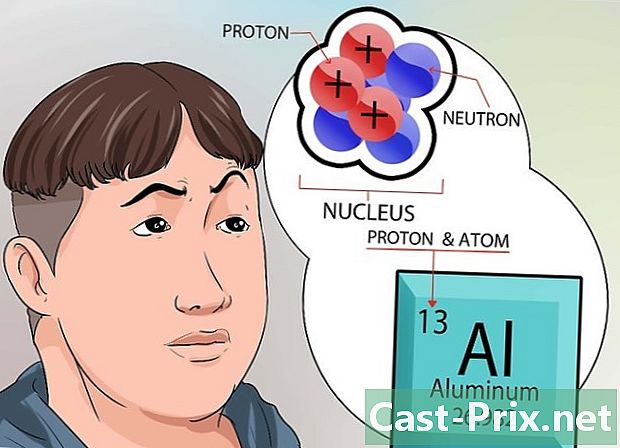
Dagdagan ang nalalaman tungkol sa kernel. Ang mga neutron, na nasa nucleus, ay may isang singil na neutral na singil. Ang mga proton, sa kabilang banda, ay may positibong singil. Ang atomic number ng isang elemento ay tumutugma nang eksakto sa bilang ng mga proton na naroroon sa nucleus nito.- Hindi mo kailangang gumawa ng isang pagkalkula ng matematika upang malaman ang bilang ng mga proton ng isang elemento. Ang halagang ito ay ipinapahiwatig sa tuktok ng bawat kahon ng bawat elemento ng pana-panahong talahanayan.
-
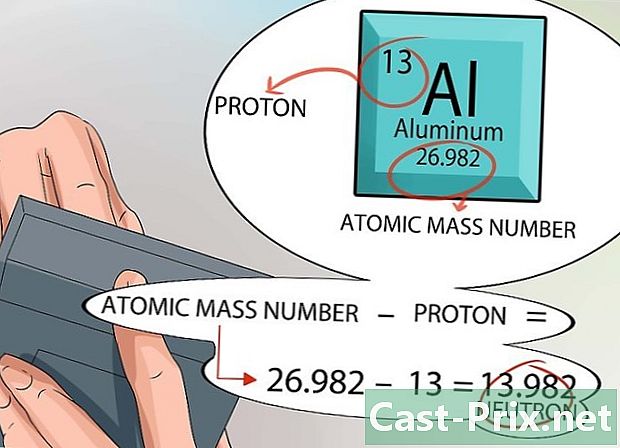
Kalkulahin ang bilang ng mga neutron sa nucleus. Maaari mong gamitin ang impormasyong ibinigay sa pana-panahong talahanayan para sa hangaring ito. Ang atomic number ng bawat elemento ay katumbas ng bilang ng mga proton sa nucleus.- Ang atomic mass ay ipinahiwatig sa bawat kahon ng pana-panahong talahanayan at nasa ilalim, sa ilalim lamang ng pangalan ng elemento.
- Tandaan na ang mga proton at neutron lamang ang nasa nucleus. Sa pana-panahong talahanayan, maaari mong malaman ang bilang ng mga proton at ang atomic mass ng isang elemento ng kemikal.
- Sa puntong ito, ang pagkalkula ay medyo simple. Ibawas lang ang bilang ng mga proton mula sa masa ng atom upang mahanap ang bilang ng mga neutron sa latome nucleus ng elementong iyon.
-
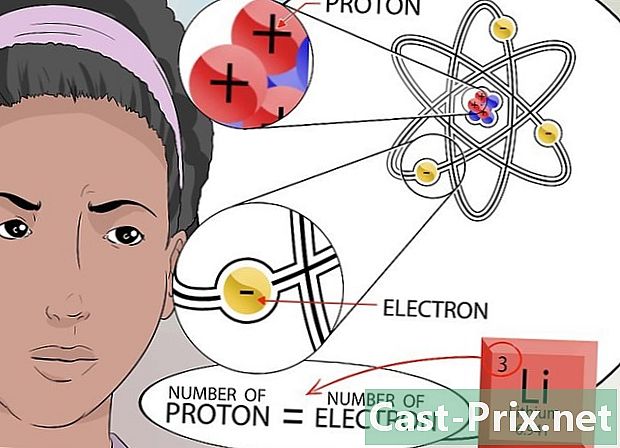
Alamin ang bilang ng mga elektron. Tandaan na ang mga kabaligtaran na elemento ay tama. Ang mga elektron ay negatibong sisingilin ng mga particle na umiikot sa nucleus, tulad ng mga planeta na umiikot sa paligid ng araw. Ang bilang ng mga elektron (na may negatibong singil) na naaakit sa nucleus ay nakasalalay sa bilang ng mga proton (na may positibong singil) na naroroon sa nucleus.- Dahil ang zero ay walang kabuuang kabuuang singil, ang lahat ng positibo at negatibong singil ay dapat na balansehin. Para sa kadahilanang ito, ang bilang ng mga electron ay katumbas ng bilang ng mga proton.
-
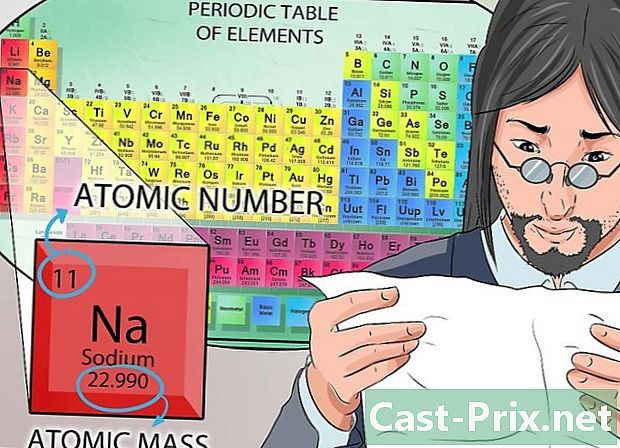
Sundin ang pana-panahong talahanayan. Kung nahihirapan kang maunawaan ang mga katangian ng mga elemento ng kemikal, gumugol ng oras upang suriin ang lahat ng impormasyon na magagamit sa pana-panahong talahanayan. Pinakamahalaga, maingat na pag-aralan ang tsart.- Ang pag-unawa sa tsart na ito ay mahalaga sa tagumpay ng unang bahagi ng iyong klase sa kimika.
- Ang pana-panahong talahanayan ay binubuo lamang ng mga elemento. Ang bawat dalawa ay kinakatawan ng isa o dalawang sagisag. Natutukoy ng simbolo ang elemento na natatangi. Halimbawa, ang simbolo Na palaging nangangahulugang sodium latome. Ang buong pangalan ng elemento ng kemikal ay karaniwang nakasulat sa ilalim ng simbolo.
- Ang atomic number ng isang simbolo ay kinakatawan ng numero na nakalimbag sa itaas nito. Ang numero ng atomic ay katumbas ng bilang ng mga proton sa nucleus.
- Ang numero sa ilalim ng simbolo ay tumutugma sa masa ng atomic. Huwag kalimutan ito: ang dami ng isang atom ay katumbas ng kabuuan ng mga proton at neutron na nakapaloob sa nucleus.
-
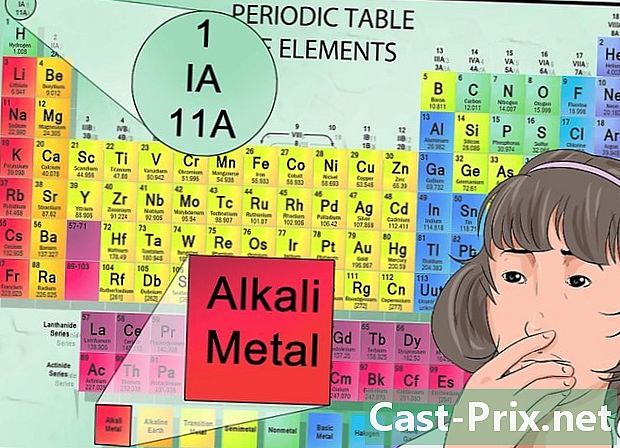
I-interpret ang pana-panahong talahanayan. Maraming impormasyon sa pana-panahong talahanayan, kabilang ang mga kulay ng bawat haligi at ang lokasyon ng mga elemento mula kaliwa hanggang kanan at mula sa itaas hanggang sa ibaba.
Bahagi 3 Pagsula ng Chemical Reaction
-

Balansehin ang isang equation ng kemikal. Sa kimika, kakailanganin mong hulaan kung ano ang reaksyon ng mga elemento sa bawat isa. Sa madaling salita, dapat mong balansehin ang isang reaksyon ng kemikal.- Sa isang equation ng kemikal, ang mga reagents ay matatagpuan sa kaliwa, na sinusundan ng isang arrow na tumuturo sa kanan na nagpapahiwatig ng mga produkto ng reaksyon. At ang mga elemento sa bawat panig ng equation ay dapat balanseng.
- Halimbawa, Reagent 1 + Reagent 2 → Product 1 + Product 2.
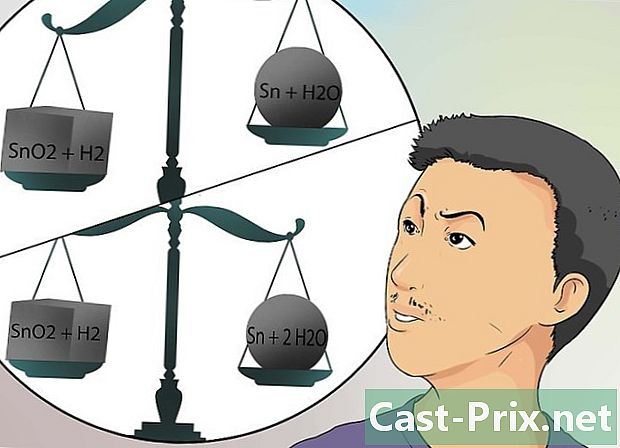
- Narito ang isang halimbawa na may mga simbolo ng lata, na ang simbolo ay Sn. Pagsamahin ang tin dioxide (SnO2) na may hydrogen sa gas na form (H2). Ang equation ay SnO2 + H2 → Sn + H2O.
- Gayunpaman, ang equation na ito ay hindi balanseng, dahil ang dami ng reagents ay hindi katumbas ng sa mga produkto. May isa pang atom na oxygen sa kaliwang bahagi kaysa sa kanang bahagi ng reaksyon.
- Gamit ang simpleng mga kalkulasyon sa matematika, maaari mong balansehin ang equation sa pamamagitan ng paglalagay ng dalawang yunit ng hydrogen sa kaliwa at dalawang mga molekula ng tubig sa kanan. Ang reaksyon sa sandaling pinagsama-sama ay: SnO2 + 2 H2 → Sn + 2 H2O.
-
Mag-isip ng mga equation nang magkakaiba. Kung nagkakaproblema ka sa pagbabalanse ng mga reaksyon ng kemikal, isipin kung anong bahagi ng isang recipe, ngunit kailangan mong gumawa ng mga pagsasaayos upang makakuha ng higit o mas kaunti ang pangwakas na produkto ng recipe.- Ang equation ay nagbibigay sa iyo ng mga sangkap sa kaliwang bahagi ng equation, ngunit hindi ka nagbibigay sa iyo ng impormasyon tungkol sa mga dosis. Gayunpaman, ang equation ay nagpapahintulot sa iyo na malaman kung ano ang iyong makukuha bilang isang produkto, palaging tinatanggal ang dami. At kailangan mong hanapin ang mga ito.
- Palaging ginagamit ang halimbawa sa itaas (ng SnO2 + H2 → Sn + H2O), isaalang-alang kung bakit hindi gumagana ang reaksyon na ito (o ang pormula ng recipe). Ang halaga ng lata (Sn) sa magkabilang panig ng ekwasyon ay pantay, pati na rin ang halaga ng hydrogen (H2). Gayunpaman, sa kaliwa mayroon kaming 2 mga atom ng oxygen at sa kanan lamang 1.
- Baguhin ang kanang bahagi ng equation upang ipahiwatig na mayroong dalawang molekula ng H2O (2 H2O). Ang numero 2 sa harap H2O nangangahulugan na ang lahat ng mga atom ng molekula na ito ay nadoble ngayon. Ngayon, ang halaga ng oxygen ay balanse, ngunit hindi ang mga hydrogen, dahil sa kanan ay may higit pang hydrogen kaysa sa kaliwa. Para sa kadahilanang ito, dapat tayong bumalik sa kaliwang bahagi ng equation. Baguhin ang dami ng sangkap H2 at doble ang mga ito sa pamamagitan ng paglalagay ng isang koepisyent 2 sa harap ng H2.
- At narito ka, binabalanse ang lahat ng mga dosis ng mga sangkap sa magkabilang panig ng equation. Ang mga sangkap ng iyong resipe ay pareho (samakatuwid ay balanse) bilang nakuha ng mga produkto.
-
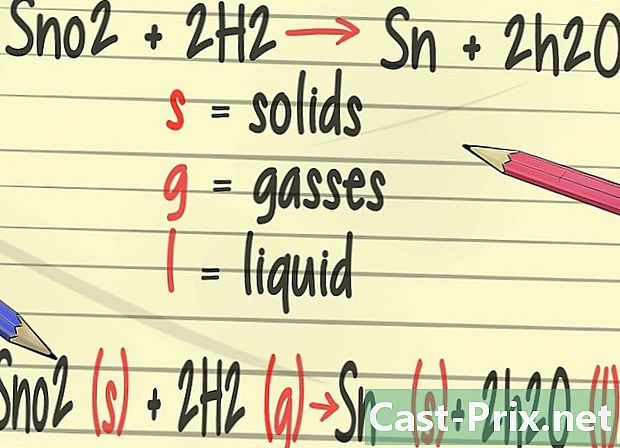
Magdagdag ng higit pang detalye sa balanseng mga equation. Sa kimika matututo kang magdagdag ng mga simbolo na kumakatawan sa pisikal na estado ng mga elemento. Ang liham s sumisimbolo ng solido, ang liham g ay ginagamit para sa mga gas at liham l ay kumakatawan sa mga likido. -
Kilalanin ang mga pagbabagong nagaganap sa panahon ng isang reaksyon. Ang mga reaksyon ng kemikal ay unang nakakaapekto sa mga pangunahing elemento o pinagsama na mga elemento na tinatawag na mga reagents. Ang kumbinasyon ng dalawa o higit pang mga reagents ay humahantong sa isa o higit pang mga produkto.- Upang makapasa ng isang pagsusulit sa kimika, dapat mong malutas ang mga equation na nagsasangkot ng mga reagents, produkto, at isinasaalang-alang ang iba pang mga kadahilanan na nakakaimpluwensya sa kanilang pag-uugali.
-
Pag-aralan ang iba't ibang uri ng reaksyon. Ang mga reaksiyong kemikal ay nangyayari dahil sa isang bilang ng mga kadahilanan na lumalampas sa tanging pagsasama-sama ng mga sangkap.- Ang mga tipikal na reaksyon na pinag-aaralan sa kimika at dapat mong malaman ay ang mga sumusunod: reaksyon ng synthesis, pagpapalit, acidobasic reaksyon, pagbabawas ng oksihenasyon, pagkasunog, hydrolysis, agnas, pagsukat at disomerization.
- Sa panahon ng klase ng kimika, ang iyong guro ay maaari ring magpakita ng iba pang mga uri ng reaksyon depende sa programa. Malinaw, ang programa ng kimika sa high school ay hindi magiging detalyado tulad ng itinuro sa programa sa unibersidad.
-

Gamitin ang lahat ng mga mapagkukunan na magagamit mo. Dapat mong makilala ang mga pagkakaiba-iba sa bawat uri ng puna na tinalakay sa klase. Gamitin ang lahat ng mga mapagkukunan ng pag-aaral na mayroon ka upang maunawaan ang mga konsepto na ito at huwag mag-atubiling magtanong sa klase.- Ang mga pagkakaiba sa pagitan ng mga reaksyon ay maaaring lumikha ng pagkalito para sa nag-aaral, at pag-unawa sa iba't ibang mga mekanismo na nagaganap sa isang reaksyon ng kemikal ay maaaring maging pinaka kumplikadong bahagi ng buong kurso.
-

Unawain nang lohikal ang mga reaksyon ng kemikal. Huwag gawing mas kumplikado ang proseso kaysa sa mayroon na, naiwan kang nalilito sa mga pangkalahatang termino. Sa lahat ng mga reaksyon na iyong pag-aaralan, kailangan mo lang gawin ang iba pa.- Halimbawa, alam mo na sa pamamagitan ng pagsasama ng dalawang molekula ng hydrogen na may isang molekula ng oxygen, nakakakuha ka ng tubig. Samakatuwid, kung ibubuhos mo ang tubig sa isang kasirola at ilagay ito sa apoy, may magbabago. Lumikha ka talaga ng isang reaksyon ng kemikal. Kung naglagay ka ng tubig sa freezer, may mangyayari din. Sa madaling sabi, ipinakilala mo ang isang kadahilanan na nagbabago sa estado ng paunang reagent at sa aming kaso ito ay tubig.
- Isulat ang bawat kategorya ng reaksyon nang paisa-isa hanggang sa makabisado mo ito, pagkatapos ay lumipat sa susunod. Tumutok sa mapagkukunan ng enerhiya na nag-trigger sa reaksyon at sa mga pangunahing pagbabago na nagaganap.
- Kung hindi mo maintindihan ang mga konsepto na ito, gumawa ng isang listahan ng lahat na hindi mo maintindihan at talakayin ito sa iyong guro, iyong pangkat ng pag-aaral, o isang taong medyo mahusay sa kimika.
Bahagi 4 Paglalapat ng Matematika sa Chemistry
-

Alamin ang pagkakasunud-sunod ng mga pangunahing kalkulasyon. Sa kimika, kung minsan ang napaka detalyadong mga kalkulasyon ay kinakailangan, ngunit sa ibang oras, ang mga pangunahing operasyon ay sapat. Gayunpaman, mahalagang malaman ang eksaktong pagkakasunud-sunod ng mga operasyon upang makumpleto at malutas ang mga equation.- Kabisaduhin ang isang acronym na medyo simple. Ang mga mag-aaral ay gumagamit ng iba't ibang mga pangungusap upang kabisaduhin ang ilang mga konsepto, at ang pagkakasunud-sunod ng mga operasyon sa matematika ay walang pagbubukod. Gamit ang pangalang PEMDAS (na nagmula sa pariralang Siguro ang Aking Huling AS), madali mong matandaan kung aling pagkakasunud-sunod upang maisagawa ang mga pagpapatakbo sa matematika. Ang unang titik ng bawat salita ay nagpapahiwatig ng pagkakasunud-sunod ng bawat operasyon. Una, gawin ang lahat sa Parentheses, pagkatapos ay Mga Exhibitor, Multiplications, Dibisyon, Pagdaragdag at sa wakas Mga Pagbabawas.
- Gawin ang mga kalkulasyon para sa expression na ito 3 + 2 x 2 x 6 = ___, kasunod ng pagkakasunud-sunod ng mga operasyon na ipinahiwatig ng pangalang PEMDAS. Ang solusyon ay 15.
-

Alamin kung paano mag-ikot ng napakalaking halaga. Bagaman ang mga numero ng pag-ikot ay hindi pangkaraniwan sa kimika, kung minsan ang solusyon sa ilang kumplikadong mga equation ng matematika ay masyadong mahaba upang magsulat. Basahin nang mabuti ang mga tagubilin ng mga pagsasanay na iyong ginagawa upang malaman kung dapat mong ikot ang iyong mga sagot o hindi.- Alamin kung kailan mag-ikot pataas o pababa. Sa sunud-sunod na pagkakasunud-sunod, kung ang susunod na numero ay mas mababa sa o katumbas ng 4, bilog. At kung ito ay higit sa o katumbas ng 5, bilugan hanggang sa susunod na numero. Isaalang-alang natin ang halimbawa ng bilang na ito 6, 66 666 666 666 666. Ipagpalagay na kailangan mong yumuko sa pangalawang lugar na desimal. Ang sagot ay magiging 6.67.
-
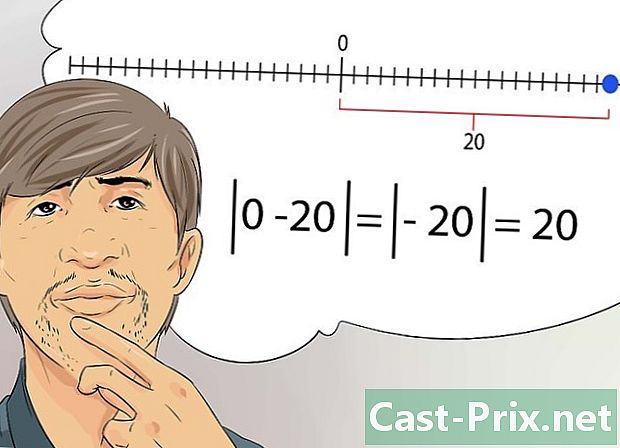
Unawain ang paniwala ng ganap na halaga. Sa kimika, ang ilang mga numero ay tinutukoy bilang mga ganap na halaga at hindi aktwal na mga halaga ng matematika. Ang ganap na halaga ng isang tunay na x ay ang distansya sa pagitan ng bilang na x at zero.- Sa madaling salita, hindi mo na kailangang isaalang-alang ang pag-sign ng numero (positibo o negatibo), ngunit sa halip ang distansya nito sa zero. Halimbawa, ang ganap na halaga ng -20 ay 20.
-
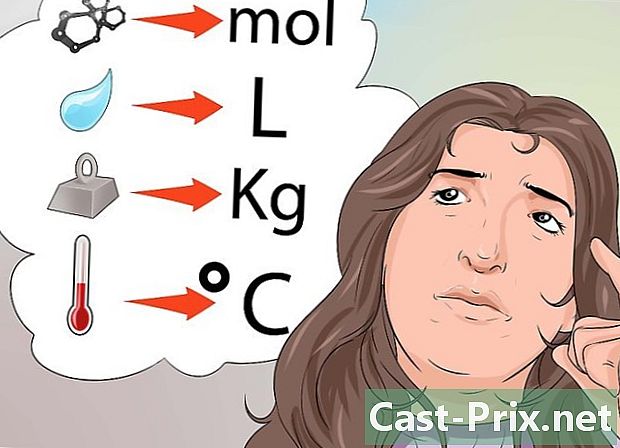
Pamilyar sa iyong tinanggap na mga yunit ng panukalang-batas. Narito ang ilang mga halimbawa.- Ang dami ng materyal ay ipinahayag sa mga moles (mol).
- Ang temperatura ay ipinahayag sa mga degree Celsius (° C), Fahrenheit (° F) o Kelvin (° K).
- Ang Mass ay ipinahayag sa gramo (g), kilograms (kg) o milligrams (mg).
- Ang dami at likido ay ipinahayag sa litro (l) o milliliter (ml).
-

Alamin kung paano i-convert ang mga halaga mula sa isang sukat sa pagsukat sa iba pa. Upang maipasa ang iyong pagsusulit sa kimika, kakailanganin mong magawa ang ilang mga pagbabagong mula sa isang tinanggap na sukat sa iba pa. Halimbawa, maaaring kailangan mong pumunta mula sa isang pagsukat ng temperatura sa isa pa, pag-convert ng mga kilo sa pounds o litro sa mga onsa ng likido.- Minsan hihilingin sa iyo na ipahayag ang solusyon ng isang problema sa isang yunit ng pagsukat na naiiba sa orihinal na yunit. Halimbawa, ipagpalagay na kailangan mong malutas ang isang equation ng temperatura na ang mga halaga ay nasa Celsius, ngunit dapat ang iyong huling sagot sa Kelvin.
- Ang Kelvin ay ang pamantayang pang-internasyonal para sa mga sukat ng temperatura na madalas na ginagamit sa mga reaksyon ng kemikal. Magsanay sa pagpunta mula sa degree Celsius hanggang degree Kelvin o degree Fahrenheit.
-
Gumugol ng ilang oras sa paggawa ng mga ehersisyo. Habang pinag-aaralan mo ang ilang mga konsepto sa klase, gumugol ng oras upang malaman kung paano i-convert ang mga yunit ng pagsukat mula sa isang sistema patungo sa isa pa. -

Alamin kung paano makalkula ang mga konsentrasyon. Palalimin ang iyong pangunahing kaalaman sa mga porsyento, proporsyon at ratios. -

Magsanay sa mga label ng nutrisyon. Upang maipasa ang iyong pagsusulit sa kimika, dapat mong madaling makalkula ang mga ratio, porsyento, proporsyon at kanilang mga kabaligtaran na operasyon. Kung hindi mo naiintindihan nang mabuti ang mga konsepto na ito, kailangan mong sanayin kasama ang iba pang mga yunit ng pagsukat na medyo pangkaraniwan, tulad ng mga nasa mga label ng nutrisyon.- Suriin ang label ng nutrisyon ng anumang produktong pagkain. Makakakita ka ng mga kaloriya sa bawat paghahatid, porsyento ng inirekumendang pang-araw-araw na paggamit, kabuuang nilalaman ng taba, porsyento ng mga calories sa taba, kabuuang karbohidrat na nilalaman, at ang pagkasira ng iba't ibang uri ng karbohidrat. Alamin kung paano makalkula ang iba't ibang mga porsyento mula sa mga halaga ng iba't ibang mga kategorya bilang mga denominador.
- Halimbawa, kalkulahin ang dami ng monounsaturated fat na nauugnay sa kabuuang halaga ng taba sa isang produkto. I-convert ang halaga sa isang porsyento. Kalkulahin ang bilang ng mga calorie sa produkto sa pamamagitan ng paggamit ng bilang ng mga kaloriya sa bawat paghahatid at ang halaga ng mga bahagi sa package. Kalkulahin ang dami ng sodium na naroroon sa kalahati ng nakabalot na produkto.
- Sa pamamagitan ng pagsasanay sa mga naturang conversion, kahit anong yunit ng pagsukat na ginagamit mo, madali mong mai-convert ang mga yunit ng sukatan sa dami ng kemikal tulad ng nunal bawat litro, gramo bawat taling, at iba pa.
-

Alamin kung paano gamitin ang bilang ng Avogadro. Ang palagiang ito ay kumakatawan sa bilang ng mga molekula, datome o mga partikulo na naglalaman ng isang nunal. Ang bilang ng Avogadro ay 6,022 x 1023.- Halimbawa, gaano karaming mga database na nasa 0.450 moles ng Fe? Ang sagot ay 0.450 x 6 022 x 1023.
-
Mag-isip ng mga karot. Kung nahihirapan kang ilapat ang bilang ng Avogadro sa mga problema sa kimika, mag-isip ng mga karot kaysa sa mga atomo, molekula o mga partikulo. Ilan ang karot sa isang dosenang? Ang isang dosenang may 12 elemento, kaya mayroong 12 karot sa isang dosenang.- Ngayon, subukang sagutin ang tanong na ito: ilang karot ang nasa mole? Sa halip na dumami ng 12, gamitin ang bilang ng Avogadro. Mayroong 6,022 x 1,023 core sa isang nunal.
- Ang bilang ng Avogadro ay ginagamit upang i-convert ang halaga ng kemikal (ang bilang ng mga moles) sa isang bilang ng mga bagay (isang atom, isang molekula, isang butil o isang karot).
- Kung alam mo ang bilang ng mga moles ng isang elemento, maaari mong malaman ang bilang ng mga molekula, mga datos o partikulo na naroroon sa dami ng bagay na ito sa pamamagitan ng pagpaparami ng patuloy na dAvogadro sa pamamagitan ng bilang ng mga moles na pinag-uusapan.
- Mahalagang maunawaan kung paano i-convert ang mga particle sa nunal upang maipasa ang iyong pagsusulit sa kimika. Upang makalkula ang mga ratio at porsyento, kailangan mong gumawa ng mga molar conversion. Sa madaling salita, dapat mong malaman ang dami ng isang sangkap na ipinahayag sa nunal kumpara sa isa pang yunit.
-
Sikaping maunawaan ang konsepto ng molarity. Isaalang-alang ang bilang ng mga moles ng isang sangkap na natunaw sa isang likidong daluyan. Ito ay isang napakahalagang halimbawa upang maunawaan sapagkat ito ay ang molaridad, iyon ang proporsyon ng isang uri ng kemikal na ipinahayag sa mga moles bawat litro.- Sa kimika, ang molarity ay ginagamit upang maipahayag ang dami ng isang sangkap na nilalaman sa isang likidong daluyan, o ang halaga ng solute na nilalaman sa isang likidong solusyon. Maaari mong kalkulahin ang molarity sa pamamagitan ng paghati sa bilang ng mga moles ng isang solusyo sa pamamagitan ng dami ng solusyon sa litro. Ang yunit ng panukala nito ay ang nunal bawat litro (mol / l).
- Kalkulahin ang density. Ang kalakal din ay isang karaniwang ginagamit na panukala sa kimika. Nagpapahayag ito ng masa sa bawat yunit ng dami ng isang kemikal na sangkap. Ang pinakakaraniwang yunit ng pagsukat dito ay ang gramo bawat litro (g / l) o ang gramo bawat kubiko sentimetro (g / cm3).
-

Bawasan ang mga equation sa kanilang empirical formula. Sa madaling salita, ang pangwakas na mga solusyon ng iyong mga equation ay maituturing na mali kung hindi mo bawasan ang mga ito sa kanilang pinakasimpleng form.- Hindi ito nalalapat sa mga formula ng molekula dahil ang ganitong uri ng paglalarawan ay nagpapahiwatig ng eksaktong sukat sa pagitan ng mga elemento ng kemikal na bumubuo ng molekula.
-

Unawain ang konsepto ng formula ng molekular. Hindi mo kailangang bawasan ang isang molekula na formula sa pinakasimpleng porma nito, o empirikal, sapagkat ipinahayag nito nang eksakto ang komposisyon ng molekula.- Upang isulat ang formula ng molekular ng isang katawan ay ang paggamit ng mga pagdadaglat ng mga elemento ng kemikal pati na rin ang bilang ng mga datos ng bawat elemento sa molekula.
- Ipagpalagay na ang formula ng molekular na tubig, H2O. Ang bawat molekula ng tubig ay nabuo ng dalawang mga atom ng hydrogen at isang atom ng oxygen. Subukan na gawin ang parehong sa molekular na formula ng Lacetaminophen, C8H9NO2. Sa katunayan, ang lahat ng mga kemikal na compound ay kinakatawan ng kanilang mga molekular na formula.
-

Dagdagan ang nalalaman tungkol sa stoichiometry. Marahil ay matutugunan mo ang term na ito. Ang Stoichiometry ay ang pag-aaral ng dami ng mga reaksyon ng kemikal na paggamit ng mga pormula sa matematika. Sa stoichiometry (matematika na inilalapat sa kimika), ang mga halaga ng mga elemento at kemikal na compound ay karaniwang kinakatawan sa mga moles, sa mga porar na porsyento, sa mga moles bawat litro o sa mga moles bawat kilo.- Ang isa sa mga pinaka-karaniwang operasyon sa matematika na gagawin mo ay ang pag-convert ng gramo sa mga mol. Ang yunit ng atomic mass ng isang elemento, na karaniwang ipinahayag sa gramo, ay tumutugma sa isang nunal ng sangkap na ito. Halimbawa, ang calcium latome mass ay 40 atomic mass unit. Kaya, 40 g ng calcium ay katumbas ng isang nunal ng calcium.
-

Hilingin sa guro para sa karagdagang mga pagsasanay. Kung ang mga equation at conversion ng matematika ay isang problema, makipag-usap sa guro. Hilingin sa kanya na bigyan ka ng mas maraming pagsasanay na gawin ang iyong sarili, hanggang sa malinaw mong maunawaan ang lahat ng mga konsepto na ginamit.
Bahagi 5 Gamit ang wika ng kimika
-
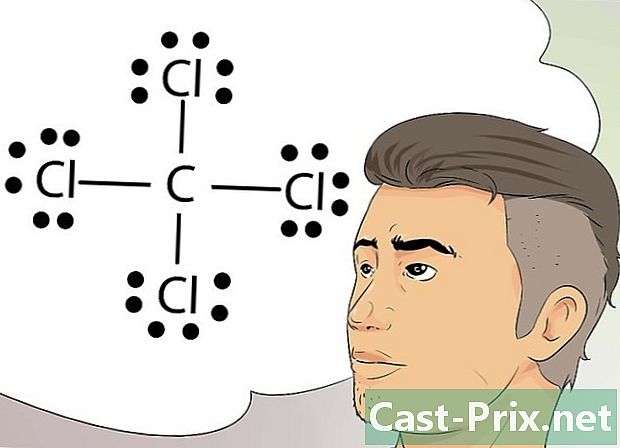
Kilalanin ang mga istruktura ni Lewis. Ang mga istrukturang ito, na tinatawag ding mga formula ng Lewis, ay mga graphical na representasyon ng paggamit ng mga tuldok upang kumatawan sa mga pinagsama-samang mga electron at solong elektron sa panlabas na layer ng isang atom.- Ang mga istrukturang ito ay napaka-kapaki-pakinabang para sa pagguhit ng mga simpleng diagram at pagkilala sa mga bono, tulad ng mga covalent bond, na ilang mga elemento ay nakikibahagi sa isang atom o isang molekula.
-

Alamin ang panuntunan ng loktet. Ang mga istruktura ng Lewis ay batay sa panuntunang ito, na nagsasaad na ang mga atomo ay matatag kapag ang kanilang panlabas na layer ay naglalaman ng eksaktong 8 elektron. Bilang isang pagbubukod sa panuntunang ito, ang hydrogen ay itinuturing na matatag na may 2 elektron sa panlabas na layer nito. -
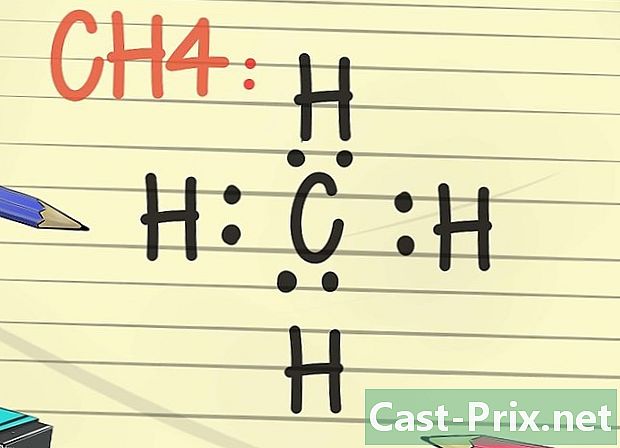
Gumuhit ng isang istraktura ng Lewis. Ang istraktura na ito ay kinakatawan ng simbolo ng isang elemento na napapaligiran ng isang serye ng mga puntos. Isipin ito ay isang nakunan pa rin ng imahe ng isang pelikula. Sa halip na ang mga electrons na gravitating sa paligid ng nucleus, kinakatawan namin ang kanilang posisyon sa isang naibigay na sandali sa oras.- Pinapayagan ng istraktura ng Lewis na mailarawan ang pinaka-matatag na pag-aayos ng mga electron, ang mga lokasyon ng kanilang koneksyon sa isa pang elemento ng kemikal. Nagbibigay din ito ng impormasyon tungkol sa lakas ng bono (halimbawa, kung sila ay covalent o doble).
- Subukang iguhit ang istruktura ng Lewis carbon (C) na isinasaalang-alang ang batas na byte. Ngayon ilagay ang 2 puntos sa bawat panig ng latome (tuktok, ibaba, kaliwa at kanan). Ngayon ay sumulat ng isang H, hydrogen latome simbolo, sa kabilang panig ng bawat pares ng mga tuldok. Ang istrakturang Lewis na ito ay kumakatawan sa isang carbon atom na napapalibutan ng apat na mga atom ng hydrogen. Kapag ang mga electron ay konektado sa pamamagitan ng isang covalent bond, nangangahulugan ito na ang carbon ay nagbabahagi ng isang elektron sa bawat hydrogen atom at nalalapat din ito sa hydrogen.
- Ang molekular na formula ng halimbawang ito ay CH4, iyon ng mitein.
-
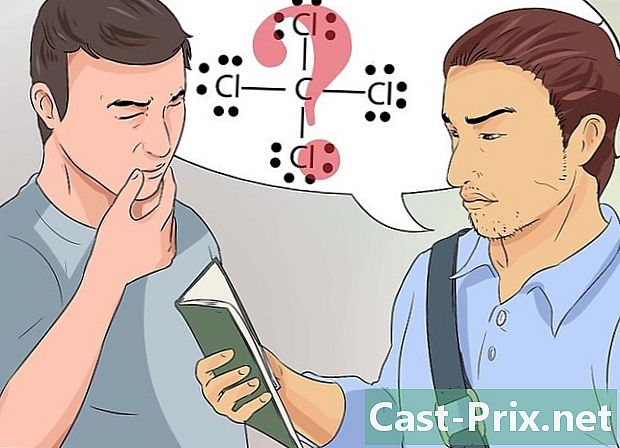
Alamin kung paano ayusin ang mga electron ayon sa kanilang bono. Ang mga istruktura ng Lewis ay isang simple na visual na representasyon ng mga bono ng kemikal.- Kung hindi mo naiintindihan ang ilang mga konsepto tungkol sa mga bono ng kemikal at mga pormula ng Lewis, talakayin ang mga ito sa iyong guro o pangkat ng pag-aaral.
-
Alamin kung paano pangalanan ang mga compound. Ang kimika ay may sariling mga patakaran tungkol sa nomenclature. Ang mga uri ng mga reaksyon na nangyayari sa isang tambalang, pagkawala o pagdaragdag ng mga electron sa panlabas na layer, at ang katatagan o kawalang-tatag ng isang tambalan ay mga kadahilanan na posible na pangalanan ang isang compound ng kemikal. -

Huwag maliitin ang nomenclature sa kimika. Sa karamihan ng mga kaso, ang mga unang kabanata sa kimika ay nakatuon sa nomenclature. Kadalasan, ang mga maling pagkilala sa mga compound ng kemikal ay maaaring mabigo kang suriin.- Kung maaari, alamin kung paano pangalanan ang mga compound ng kemikal bago simulan ang iyong kurso. Maaari kang bumili ng isang gabay o kumunsulta sa mga mapagkukunan sa online.
-
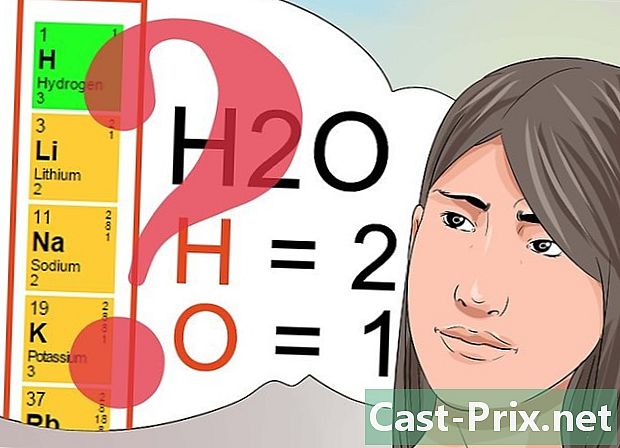
Unawain ang kahulugan ng mga numero sa superscript at subskripsyon. Mahalagang maunawaan kung ano ang ibig sabihin ng mga bilang na ito kung nais mong maipasa ang iyong pagsusulit.- Ang mga numero na inilagay sa superscript ay sumusunod sa isang pattern na lilitaw sa pana-panahong talahanayan at nagpapahiwatig ng kabuuang singil ng elemento ng kemikal o compound ng kemikal. Ulitin ang pana-panahong talahanayan at makikita mo na ang mga elemento na nakaayos sa parehong patayong haligi (pangkat) ay nagbabahagi ng parehong mga numero sa pamamagitan ng exponent.
- Ginagamit ang mga indented na numero upang matukoy ang dami ng bawat elemento na kinilala bilang bahagi ng isang compound ng kemikal. Tulad ng nabanggit sa itaas, ang index 2 ng molekula H2O ay nagpapahiwatig na mayroong dalawang mga hydrogen atoms.
-

Alamin kung paano gumanti ang mga atomo sa bawat isa. Ang bahagi ng nomenclature na ginamit sa kimika ay may kasamang mga tukoy na patakaran sa pagbibigay ng pangalan ng mga produktong mula sa ilang mga uri ng reaksyon.- Ang isa sa mga reaksyon na ito ay ang reaksyon ng pagbabawas ng oksihenasyon. Ito ay isang reaksyon kung saan nakuha o nawala ang mga electron.
- Upang matandaan ang mekanismo na nangyayari sa panahon ng isang reaksyon ng doxydoreduction, kabisaduhin ang pangalan RROO. Ito ay isang simpleng paraan upang matandaan iyon Gumagawa ang Reducer ng Mga Elektron Habang Nakakuha ang Oxidant.
-
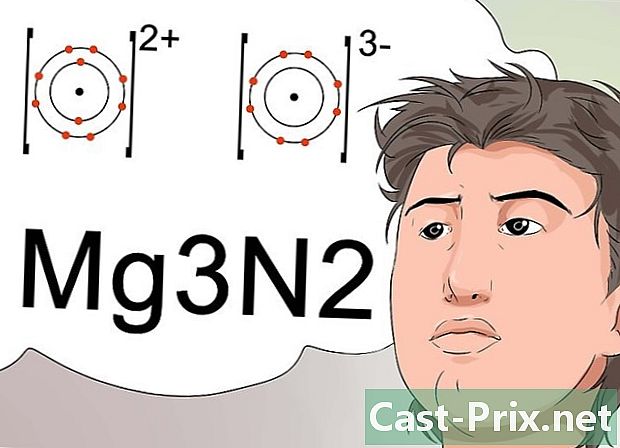
Gamitin ang mga numero sa mga pahiwatig upang makakuha ng isang neutral na molekula. Gumagamit ang mga siyentipiko ng mga pahiwatig upang matukoy ang tiyak na molekular na pormula ng isang tambalan, at ipinapahiwatig din nito na ang isang compound ay matatag na may isang neutral na singil.- Upang makarating sa isang matatag na pagsasaayos ng elektronik, ang positibong ion (cation) ay dapat na mabayaran sa pamamagitan ng isang negatibong ion (anion) ng pantay na intensity. Ang mga exhibitors ay kumakatawan sa mga naglo-load.
- Halimbawa, ang lion magnesium ay nagdadala ng isang positibong singil ng +2 at ang leon nitrogen ay may negatibong singil ng -3. Ang mga numero +2 at -3 ay dapat ilagay sa superscript. Upang pagsamahin ang dalawang elemento nang naaangkop upang makakuha ng isang neutral na molekula, kinakailangan na gumamit ng 3 magnesium atoms para sa 2 mga nitrogen atom.
- Ang molekula na nakuha ay samakatuwid Mg3N2.
-
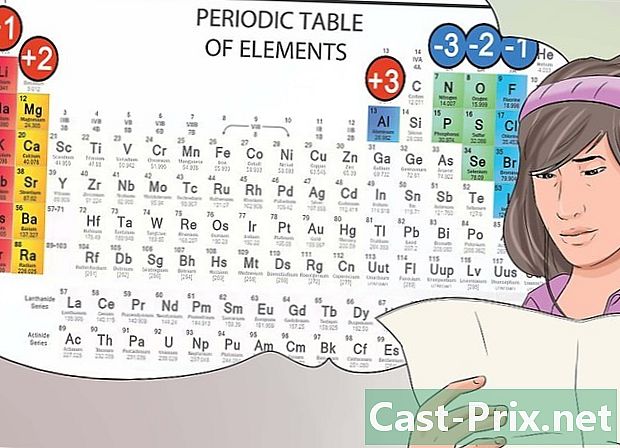
Kilalanin ang mga anion at cations mula sa kanilang posisyon. Sa pana-panahong talahanayan, ang mga elemento na kabilang sa unang pangkat ay itinuturing na mga metal na alkali at may positibong singil ng +1. Ang sodium (Na +) at lithium (Li +) ay mga halimbawa.- Ang mga alkalina na metal na metal ay bahagi ng pangalawang pangkat at bumubuo ng 2+ cations, tulad ng magnesium (Mg2 +) at barium (Ba2 +).
- Ang mga elemento ng kemikal na kabilang sa ikapitong haligi ng pana-panahong talahanayan ay bumubuo sa pamilya ng mga halogens at bumubuo ng mga anion na may negatibong singil - tulad ng chlorine (Cl-) at liode (I-).
-

Kilalanin ang pinakakaraniwang mga cations at anion. Upang magtagumpay sa iyong pagsusulit sa kimika, kakailanganin mong malaman hangga't maaari ang nomenclature ng mga pangkat ng mga elemento na hindi nagbabago ang mga numero sa exponent.- Sa madaling salita, ang magnesiyo ay palaging kinakatawan ng Mg at palaging mayroong +2 positibong singil.
-

Subukan na huwag palagpasin ang iyong sarili sa impormasyon. Hindi madaling maunawaan at tandaan ang lahat ng detalyadong impormasyon sa iba't ibang reaksyon ng kemikal, palitan ng elektron at ang pagbabago ng singil ng kuryente ng isang elemento o isang tambalan.- Ipahayag ang mga paksang hindi mo maintindihan sa mga salitang naglalarawan. Halimbawa, kung hindi mo maintindihan ang mga reaksyon ng oksihenasyon o kung paano pinagsama ang mga elemento sa negatibo at positibong singil, sabihin ito. Sa pamamagitan ng malinaw na pagpapahayag ng mga konsepto at konsepto na may problema sa iyo, maaari mong mapansin na mayroon kang maraming kontrol sa mga bagay.
-

Kilalanin nang regular ang iyong guro. Lumikha ng isang listahan ng mga paksa na hindi mo maintindihan at humingi ng tulong sa iyong guro. Ito ay isang pagkakataon upang ma-assimilate ang mga kumplikadong konsepto bago ka magpasok ng mas kumplikado at mahirap maunawaan na mga konsepto sa silid-aralan. -

Sabihin sa iyong sarili na natututo ka ng isang bagong wika. Unawain na ang mga formula na isinulat upang ipahiwatig ang mga singil, ang bilang ng mga datum sa isang molekula at ang mga bono na nabuo sa pagitan ng mga molekula ay bahagi ng wika ng kimika. Ito ay isang paraan ng kumakatawan sa mga graphic at sa pagsulat ng iba't ibang mga pagbabagong nagaganap sa isang reaksyon ng kemikal, na hindi natin nakikita.- Mas madaling maunawaan ang kimika kung ang lahat ng mga mekanismo ay maaaring maobserbahan gamit ang hubad na mata.Gayunpaman, dapat kang magsikap na maunawaan ang terminolohiya na ginamit sa kimika upang ilarawan ang mga phenomena, pati na rin ang mga mekanismo ng mga reaksyon.
- Kung nahihirapan kang maunawaan ang klase ng kimika, alamin na hindi ka nag-iisa. Gayunpaman, huwag magpaloko. Makipag-usap sa iyong guro, mag-aral sa isang pangkat, makipag-ugnay sa katulong ng iyong guro o humingi ng tulong sa isang taong talagang mahusay sa kimika. Maaari mong malaman ang buong kurso, ngunit masarap na humingi ng tulong upang maipaliwanag namin ito sa iyo upang higit mong maunawaan ang ilang mga kabanata.

